이 누리집은 대한민국 공식 전자정부 누리집입니다.
메뉴
전체메뉴
연구사업
연구자원
연구성과
알림자료
연구원 소개
누리집모음
연구사업
연구자원
- 바이오자원
- 데이터 · 지식자원
- 임상연구지원 · 시설
연구자원
국립줄기세포재생센터
- 수정일
- 2024-09-26
GMP 생산 시설
-
설립 및 운영 근거
- (설립근거) 생명공학 연구개발 활성화 및 산업적 응용촉진에 대한 지원(생명공학육성법 제11조)
- (운영 근거) 국립줄기세포재생센터 제조시설 운영 규정(질병관리청 예규 제39호)
-
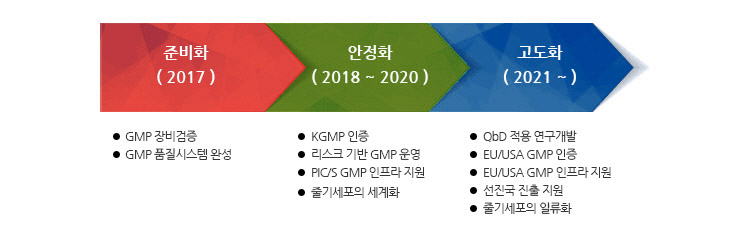
사업 추진 전략
- (준비화 단계, 2017) GMP 제조시설을 활용한 생산 준비를 위하여 선진 PIC/S GMP에 부합한 하드웨어 및 소프트웨어 구축
- (안정화 단계, 2018~2020) GMP 제조시설을 활용한 대외 운영이 원활하게 진행될 수 있도록 충분한 인프라 확충 및 적용
- (고도화 단계, 2021~2023) 축적된 경험과 기술을 기반으로 유럽 또는 미국에서 요구되는 GMP 수준까지 향상시켜 국제무대에서 선도적인 역할 수행
-
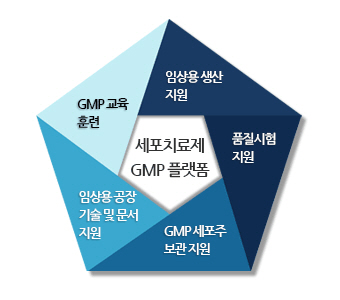
GMP 플랫폼 기능
-
임상시험용 세포치료제 위수탁 제조 및 공급 지원
- · 임상시험에 적용할 수 있는 세포치료제를 연구자로부터 기술이전을 거쳐 센터 내 3개의 독립된 GMP 생산시설에서 제조하여 공급 가능
-
임상시험용 세포치료제 위수탁 품질시험 지원
- · 세포치료제 품질시험 중 공정서에 수재된 일반시험법(무균, 미생물, 바이러스)과 제품별 특화된 세포치료제 시험방법을 GMP 시설 내에서 확립, 검증한 후 위수탁 품질 시험 지원 가능
-
GMP 세포주 위수탁 보관 관리
- · GMP 제조시설에서 제조한 세포주를 수증기 형태의 액체질소탱크에 위수탁 보관 관리 가능
-
GMP 교육 및 교육 지원
- · 세포치료제 GMP 인력 양성에 필요한 현장 중심형 교육 프로그램 개발 및 교육 사업 추진
- · 찾아가는 세포치료제 관련 GMP 교육 서비스 실시
-
임상시험 관련 기술 및 문서화 지원
- · 임상시험 제조 공정 및 시험법 개발과 관련한 기술 지원 가능
- · 임상시험 추진을 위하여 필요한 임상시험계획서(IND) 자료 작성 지원
-
임상시험용 세포치료제 위수탁 제조 및 공급 지원
-
추진 경과 및 현황
GMP 생산 시설 추진 경과 및 현황의 일정, 추진사항으로 구성 일정 추진사항 2006.05. 줄기세포연구 종합추진계획 수립 2012.07. 국립줄기세포재생센터 건립 기본 계획 수립 2013.12. 국립줄기세포재생센터 착공 2016.04. 국립줄기세포재생센터 준공 2016.10. 국립줄기세포재생센터 개소 2017.11. 식약처로부터 GMP 시설 운영 점검 실시 2018.01.~ 05. 임상시험용 제품 시범생산을 통한 GMP 생산 지원 준비 2018.05~ 본격적 임상시험용 제품 생산 지원 -
제조 시설 특징
-
기능성, 효율성, 비용, 선진 GMP 기준을 고려한 설계 적용
- * 3개의 생산시설을 독립적으로 운영할 수 있어 3개 품목을 동시 생산 가능
- ** 주요 시설 및 장비에 무정전장치(UPS)와 비상발전기(EPS)를 연결하여 생산 실패 위험 예방
-
외부 오염 및 교차 오염 예방을 고려한 설계 적용
- * 생산구역, 품질시험구역 및 세포주 보관구역에 개별 출입구를 마련하여 독립구조로 운영함으로써 오염 예방
-
기능성, 효율성, 비용, 선진 GMP 기준을 고려한 설계 적용
-
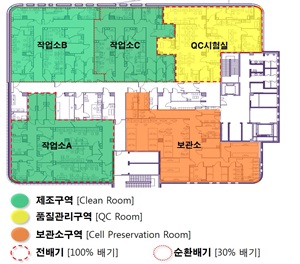
제조 시설 구조 및 용도
-
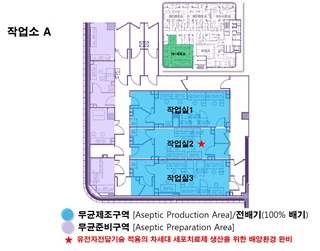
제1작업소(작업소 A)
- · 바이러스를 이용한 역분화줄기세포(iPSC) 수립 및 제조를 위한 시설로서 100% 전배기 공조시스템과 음압 유지
- · 향후 수요를 고려하여 세포유전자치료제도 제조 지원 가능
-
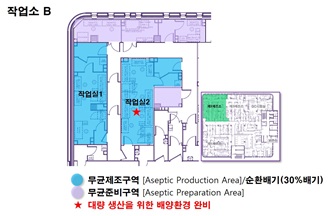
제2작업소(작업소 B)
- · 성체줄기세포를 이용한 세포치료제를 제조하는 시설로서 2개의 무균 작업실 확보
-
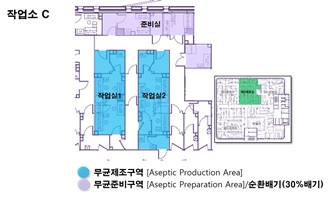
제3작업소(작업소 C)
- · 성체줄기세포를 이용한 세포치료제를 제조하는 시설로서 2개의 무균 작업실 확보
-
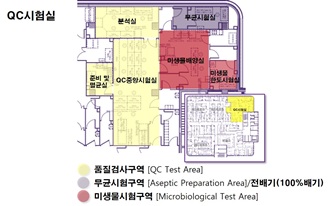
QC 시험실
- · 세포주의 공정시험 및 제품시험을 실시할 수 있는 중앙시험실과 미생물, 무균시험을 할 수 있는 청정시험실 확보
-
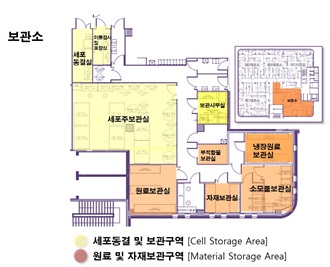
세포주 보관소
- · 자동화 액체질소 공급 시스템에 공급받은 수증기 형태의 액체질소 탱크에 품목별, 위탁 기관별, 공정 단계별로 개별 보관 가능한 다량의 세포주보 관탱크 확보
-
제1작업소(작업소 A)
-
주요 GMP 장비 보유 현황
주요 GMP 장비 보유 현황의 구분, 종류, 수량으로 구성 구분 종류 수량 제조지원설비 공기조화시스템,빌딩자동화시스템(BMS), 온도모니터링시스템(TMS), 자동환경모니터링시스템(PMS), 액체질소공급시스템 등 11종45대 제조공정장비 생물안전케비닛(BSC), CO2 배양기, 원심분리기, 역상현미경, 세포동결기(CRF) 등 20종104대 품질시험장비 형광현미경, 세포분석기(FACS), 엔도톡신분석기, 유전자증폭기(PCR), 세포수측정기, 자동핵산추출기, 부유입자측정기, 부유균포집기 등 33종71대 보관관리장비 LN2액체질소탱크, 세포주보관탱크, 초저온 냉동고, 냉동고, 냉장고 등 4종 23개 누계 68종 242대


